�����W�����z�w�S����3D��ӡ�����е��ļ���������
�r�g��2024-01-05 13:55 ��Դ��GK�G�����Ƽ� ���ߣ�admin ��x����

WHAT����ʲô�����z�w�S��
���z�w�S��һ�N�ϳ��w�S��ͨ�������z��ԭ���Ƴɣ������c��Ȼ���zԭ�w�S����������ߴ�ͨ����1.3 ��m��8.7 ��m֮�g���@�N�w�S�����^�õ����W���ܣ������cijЩ�����������õ������ԡ����z�w�S�c�w�S����������ԭ�����������ͻ��W����ã��������w�S֮�g�Ľ��|��e����߽Y�ϵď��ȡ�
WHY������ʲôҪ������3D��ӡ�ķ������������K�M����
Ŀǰ�о��ˆT������ͨ�^���|ӡˢ����̡������������w�S���z������оƬ������OӋ���K�M�������@Щ������������ȫ�������K���ܵď��s�νM�������������ܵ����ơ�������3D��ӡ�ă��ݾ������܉�������s�����������Ը����ĽY�������Ծ��_�؏��Ƽ����ͽM����ԭʼ�Y����
HOW��������ͨ�^�����z�w�Sע�����z�ͺ������}(Gel-Alg)ˮ���z���|���OӋīˮ��
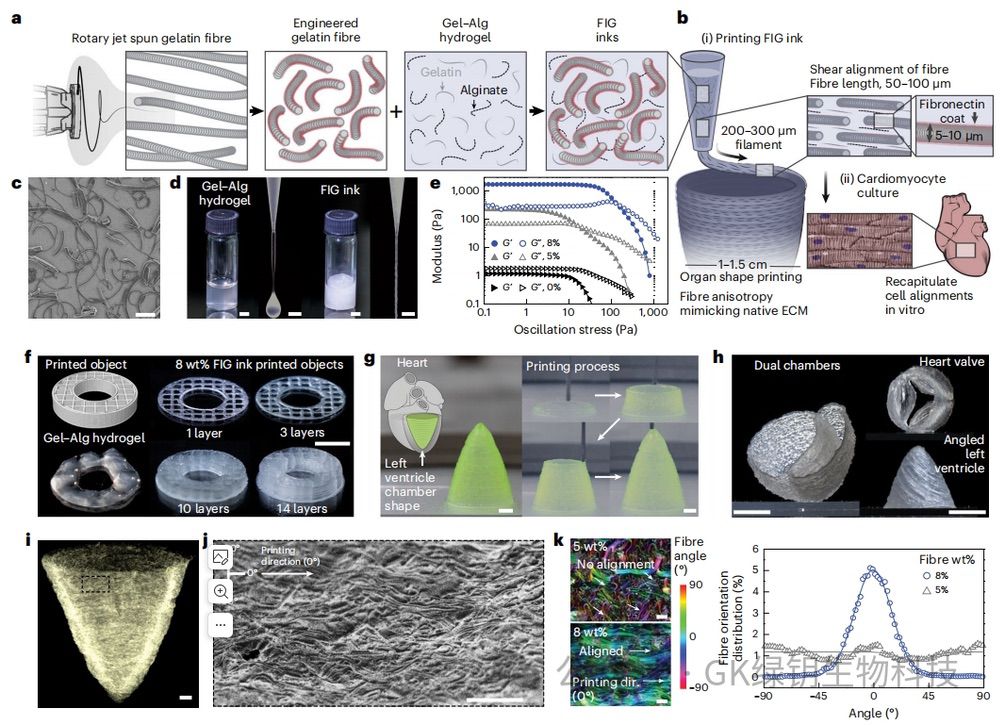
�D1 �_�l��ӡ���м������R�����Ī���ʽ3D��ӡ�M��֧�ܵ����zīˮ
���w�S����ˮ���z�п��Ը�׃īˮ����׃�ԣ��Ķ��o���κ�֧�νY������ϼ��Ʉ������_�ҏ��s��3D֧�ܡ�ͨ�^�������z�w�S����ʽ���Y���ؓ�ͻ��W��������ӡ��3D����֧���ܴ��M�ļ������ԽM���ɸ����Լ���M�����������w�Sע�����z(FIG)īˮ�����ߴ�ӡ�������z�w�S��Gel-Algˮ���z�M�ɵ�3D֧�ܡ��ڴ�ӡ�^���У�����ȵļ��Б�������ʹ���Џ��Ե�FIGīˮ׃��Һ�w���D����֏��䏗�Է����ԡ��@Щ�Ǿ�����׃�������SFIGīˮ�B�m�D����߀�܉��ӡ���s�Ď��Π�ķӽY�����ҟo������ӻ����ԡ����֧�νY�������F����֧�εĿ���3D�Y������֮�����z��FIGīˮ�ĸߏ���ģ���ṩ���������z�����ԣ����Դ�ӡ�����200 ��m��350 ��m֮�g����֧�αڣ�������Ҫ֧�ܻ����ԡ��
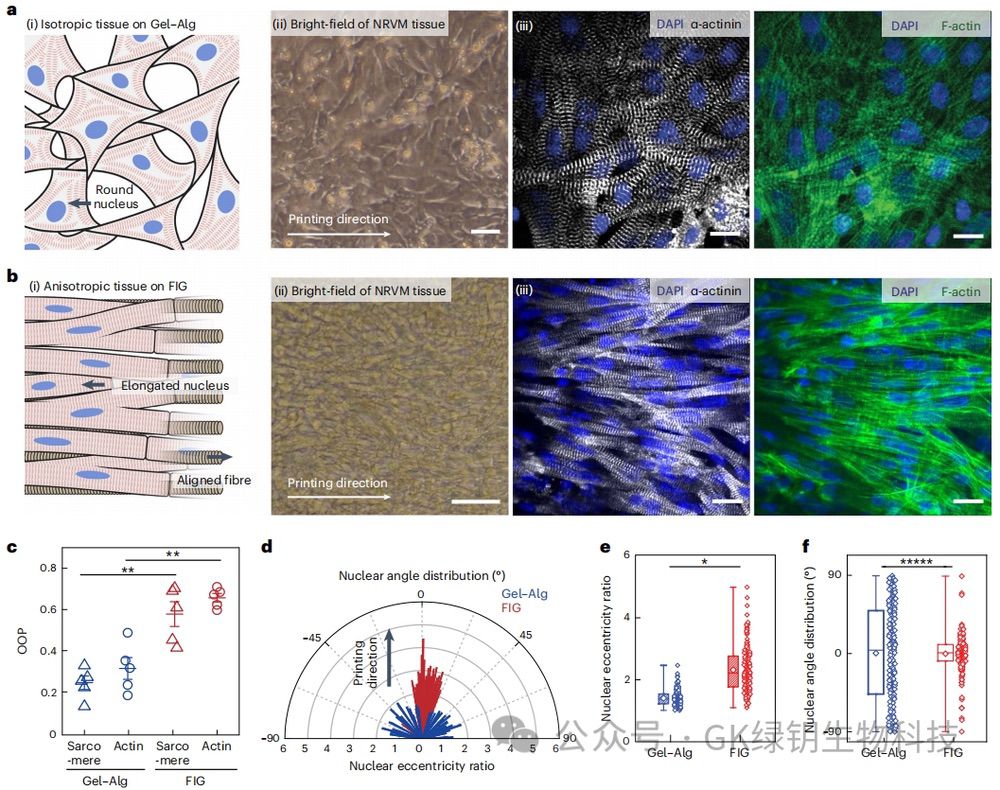
�D2 �����z�w�S��ע���z�Ĵ�ӡ֧���ϣ����B���K�M���ĸ����Լ����Ⱥͼ����g�M��
�����u��FIGīˮ��ӡ֧���������ļ������ļ����Ⱥͼ����g�M������ԭ�w�S�M�������е����������ߌ��������������ļ�������NRVM���ӷN�ڴ�ӡ�Ķ��S��2D��FIG֧���ϡ��Y���õ��߶����е����K�M�����γɣ������ڶ��������B�l���������ஔ�ļ�����������������ͨ�^Ӌ��ȡ�����(OOP)��y���Y���M���ĸ����Գ̶ȣ�ԓ���������˼����w ��-���ӵ��ͼ����Ǽܼ��ӵ��z(F -���ӵ���)���С������Ⱥͼ����g�ǼܽY���a�����A�����Q���˼����˵����L��ȡ���c����Gel-Alg֧���ϵļ�������ȣ�FIG֧���ϵļ����˱����L��NRVM�ĺ�ȡ��Ҳ�ش�ӡ��������(0��)����Gel-Alg֧�ܵĺ�ȡ��o�خ���ȡ��
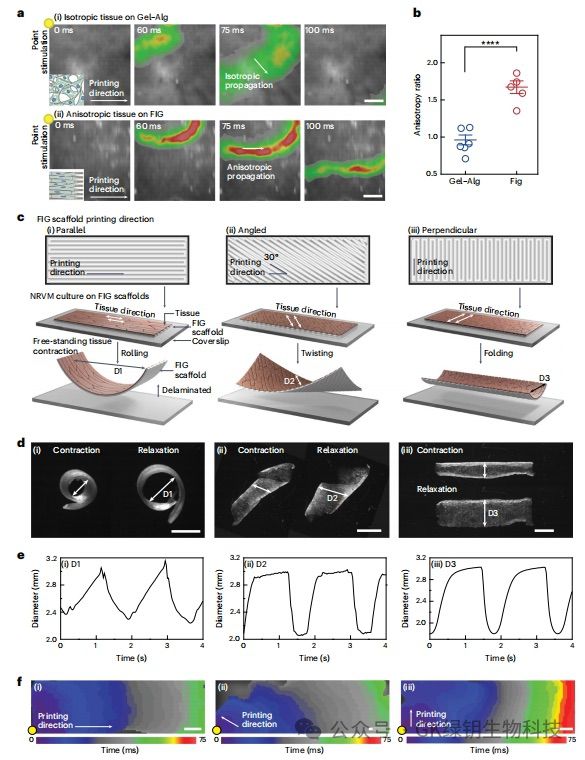
�D3 ������������K�M���ęC���τ����W
���˜yԇFIGs�T���ļ��������w�S�Y���ԽM�����γ����K���ܺϰ��w�����������ߜy������-�����B�ӽY���Ĺ��ܺ��������������ԡ�����ʹ�ù�W���D��y���}(Ca2+)˲�B���������������ڴ�ӡ�����ؿv��͙M���S�����K�}�_������ָ�ˡ����Y��������FIG֧���ϵ����K�M����6�������ΈD���ς���Ca2+�����@ʾ���ش�ӡ����ď������ϡ�����NRVM�����T�����ܸɼ���Դ���ļ�����(hiPSC-CMs)��FIG֧���Ϙ������K�M���ęM�v�����ٶ�ֵ�քe��1.67��0.085��1.62��0.18�����֮�£��]���w�S�Č���֧���ϵ�NRVM�M���Ă����ٶȱȽӽ�1���ļ������ش�ӡ����ă��șC����ʹ����늴̼��®a��ѭ�h׃�Σ���һ��֧���н������з���Ҳ�����ļ������M����ѭ�ֲ��w�S�����������ľֲ��M���տsģʽ��
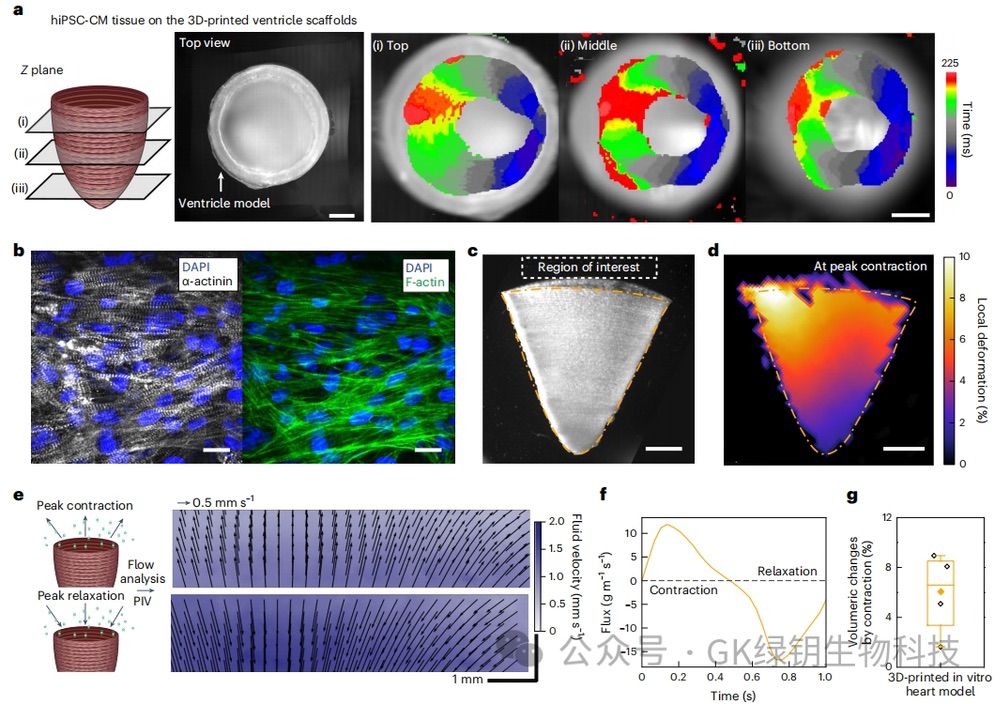
�D4 ������ɼ����ĽM�����̣����S����ģ�͵ĽY������������տs����
������3D��ӡ������֧�������BNRVM��hiPSC-CMs���w�S�ʈA�����У��γ����S�����Π�ČӠ���������K�M�����w������ģ�������B�б���14�죬�l�����ʞ�ÿ��~0.71�Ρ��@����ԓ֧���ڳ��^80�f�εęCе�d��ѭ�h�������õģ��]�����@���˻��������ڌ�NRVM���B���X��ģ���M���c늴̼����^�쵽Ca2+�ڙM��(��ӡ����)��˲�r�����ٶȱȿv����졣�@�C����3D��ӡ�X��֧���е��}�_����Ҳ�����M�����аl�����@���ɴ�ӡ����Q���ġ������u��hiPSC-CM����ģ�͵��տs���ܣ�����ʹ�����ӳ���y�� (PIV) �y���˻����_��̎�����w�����Wݔ�����������ķ�����ٶ�ʹ�܉��Ӌ�տs���ɳ����g���w�\�ӵ��|��ͨ�������Ӌ���hiPSC-CM ���B����ģ�͵������ݷe�ڷ�ֵ�տs�ͷ�ֵ�揈֮�g��׃����5.94��1.66%������ǰ�����NRVM��hiPSC-CM�w������ģ�͵Ĕ�ֵ(��Ѫ�֔�)�քe�߳�2-5����8-20����
�YՓ������չʾ���û���ˮ���z��FIGīˮ3D��ӡ�M����������ģ�͵�������ԓģ��ͬ�r�٬F�����K���Y��ECM�Y���ͺ��^�Y������ˮƽ���Πע�����z�w�S��ˮ���zīˮ�г䮔��׃���Ԅ����܉��ڲ�ʹ�à���ԡ����r�´�ӡ���s��3D���w���@Щ�w�S߀�ṩ�������^�Y�����������M����ճ�����ԽM���ɞ鹦���Ժϰ��w���@헹�������FIGīˮ��ӡ���ڴ��M�˜ʻ��Ϳ��L���������ӡ�^���аl�]��Ҫ���ã����Y�������٬F��Ȼ���َ��Π
ԭ��朽ӣ�https://doi.org/10.1038/s41563-023-01611-3
(؟�ξ���admin)
��һƪ����ʡ�����о��ˆT���y�|�V�x3D��ӡ�;��ܽM��
��һƪ��Natrx �� Danos����ɺ����3D��ӡ���a���ģ����ڱ��o�غ����B�h��
��һƪ��Natrx �� Danos����ɺ����3D��ӡ���a���ģ����ڱ��o�غ����B�h��
������
- ��649��Ԫ��Revopointȫ��MetroX 3D����
- ��649��Ԫ��Revopointȫ��Revopoint Metr
- ���K�����������WԺ�Ƴ�����3D��ӡģ��
- ���F���������F���t��Ժ�ǿ��[���F꠳ɹ�
- ���㽭ʡ�����tԺ/�㽭��W�Fꠣ����ܸ�
- ��ADNOC Gasʹ��3D��ӡ���������P�I��Q
- ��SpaceX��������Ş����ل��o䛣�����3D
- �����a�մ�3D��ӡ�˹����ޏͣ������Ƽ���
- ��3D��ӡ�����NƬ������С���ӡ�����
- ������é˹ˇ�g��W�W����������������
���c����
- ��3D��ӡ��������3D��ӡ�P���������ij���
- ����3D��ӡ�C�����b���ˣ�����3d��ӡ��һ
- ���Լ�������һ�_ֻ��20��Ԫ��3D��ӡ��
- ���֙C��ע���ˣ��Ø�ݮ��+3D��ӡ�C����
- ���P�c3D��ӡ���ޏ�������E�еĽ��䰸��
- ���D�⣺3D��ӡ�������a����
- ��SOLS��˾�l���ɶ��Ƶ�3D��ӡ�C��Ь�|
- ��ӯ��3D��ӡ�������䰸������
- ��10�����ص�3D��ӡ���裬����һ������ϲ
- ��3D��ӡ���҃��b�đ��ã��cȼ�㌦���g


 649��Ԫ��Revopointȫ��Me
649��Ԫ��Revopointȫ��Me 649��Ԫ��Revopointȫ��Re
649��Ԫ��Revopointȫ��Re �K�����������WԺ�Ƴ���
�K�����������WԺ�Ƴ��� �F���������F���t��Ժ�ǿ�
�F���������F���t��Ժ�ǿ� �㽭ʡ�����tԺ/�㽭��W
�㽭ʡ�����tԺ/�㽭��W ADNOC Gasʹ��3D��ӡ����
ADNOC Gasʹ��3D��ӡ���� �炐�ȁ���W����
�炐�ȁ���W���� ʧȥ1/3����,���
ʧȥ1/3����,��� 3D��ӡܛƤ�|����
3D��ӡܛƤ�|���� 3D��ӡ��Q������
3D��ӡ��Q������ ���ܲ����¡����T
���ܲ����¡����T �����\��Ʒ��Jack
�����\��Ʒ��Jack

