�۶�����W�_�l(f��)3D��ӡ�˹�Ѫ�ܣ����ڸ�����Ѫ�ܼ����ί�Ч��
�r�g��2024-07-30 09:58 ��Դ���ϘO�� ���ߣ�admin ��x����
2024��7��29�����Ԑ۶�����W�c�������ش�W���о��ˆT����һ�N�����ϔD����ӡ��늼��z���g(sh��)�_�l(f��)������3D ��ӡѪ����ּ��ȡ��Ŀǰ���g(sh��)��ʹ�õ����w�ͺϳ��o�}�����ڸ�׃ѪҺ����·����

��3D ��ӡѪ�ܡ��DƬ��Դ���۶�����W Norbert Radacsi ��ʿ��
�@��о����}�顰Fabrication of a Compliant VascularGraft Using
Extrusion Printing and Electrospinning
Technique/���ÔD����ӡ���o늼��z���g(sh��)����협���Ѫ����ֲ���Փ�İl(f��)���ڡ�Advanced Materials
Technologies���ڿ��ϡ�

���P(gu��n)Փ��朽ӣ�https://onlinelibrary.wiley.com/doi/10.1002/admt.202400224
��Ѫ�ܼ�����Ȼ��ȫ����Ҫ������ԭ�����Сֱ��Ѫ����ֲ�����ί���Ѫ�ܼ��������������ܴ���ͻ������Ѫ�ܼ��������ڠ���}���������܄��}�����������}����ͨ���M��Ѫ���ؽ����g(sh��)���������g(sh��)����ʹ��Ѫ�܌�������������Ӱ푻��������}�܇���Ѫ�������w��ֲ������[�o�}�����(n��i)���}�͘���}����Ȼ�Ǵ�����g(sh��)���S��˜ʣ���ʧ���ʺܸߣ�������ֲ��ɼ���(j��ng)�����¹��w��λ�l(f��)���ʡ����⣬�@Щ���w��ֲ���ڳߴ��Cе���ܷ����������ѵġ������(sh��)�ɺϳɲ��ϣ�����
Dacron �� ePTFE���Ƴɵ�������ֲ���m���ڴ�ֱ�����}��>6
���ף���Ȼ�������Á����Сֱ�����}�r���������������Ⱦ�̓�(n��i)Ĥ������ʧ����
��ˣ��۶�����W�_�l(f��)��һ�N�����p��Ѫ����ֲ����·������о��ˆT������һ�N��������ӡ���o늼��z�b�ã�����������F(xi��n)���ӽ���Ȼ���}���������W���Եķ���ֲ�
��(j��)�۶�����W�Q��3D ��ӡѪ���c���w�o�}�����Էdz����ƣ������ص�׃��Ѫ�ܼ������ί��������@Щ�Թ̡����g�����z��Ĺ��Ӳ������� 3D ��ӡ���g(sh��)������ɣ�����ȡ��Ŀǰ���g(sh��)�����ڸ�׃Ѫ����������w�������o�}���Ķ��@���������K������g(sh��)���ߵ��ί�Ч����
����Ѫ�ܵ��_�l(f��)�����ڜp���ڴ�����g(sh��)���г����w�o�}�r�a(ch��n)���İ̺ۡ���ʹ��Ⱦ�L�U��ÿ��Ӣ����s�� 20,000 ��������g(sh��)�����⣬�@Щ�a(ch��n)Ʒ�����ھ���С��������ֲ��ʧ�����L�U������@Щ��ֲ����y�������w��
���˹�Ѫ�ܵ������^���У��۶�����W���̌WԺ�I(l��ng)�����о�С�M���ü����� 3D ��ӡ�C�е����D(zhu��n)���S����ˮ�����z��������ܠ���ֲ�Ȼ��ʹ���o늼��z���g(sh��)����ӡ����ֲ���M�мӹ̣��o늼��z���g(sh��)���ø߉������dz����ļ{���w�S - �������オ��ľ������Ӱ���������Ѫ���С��Cе���ܺ��������ܜyԇ��������K�a(ch��n)Ʒ�c��ȻѪ��һ�ӈԹ̡�
���D1
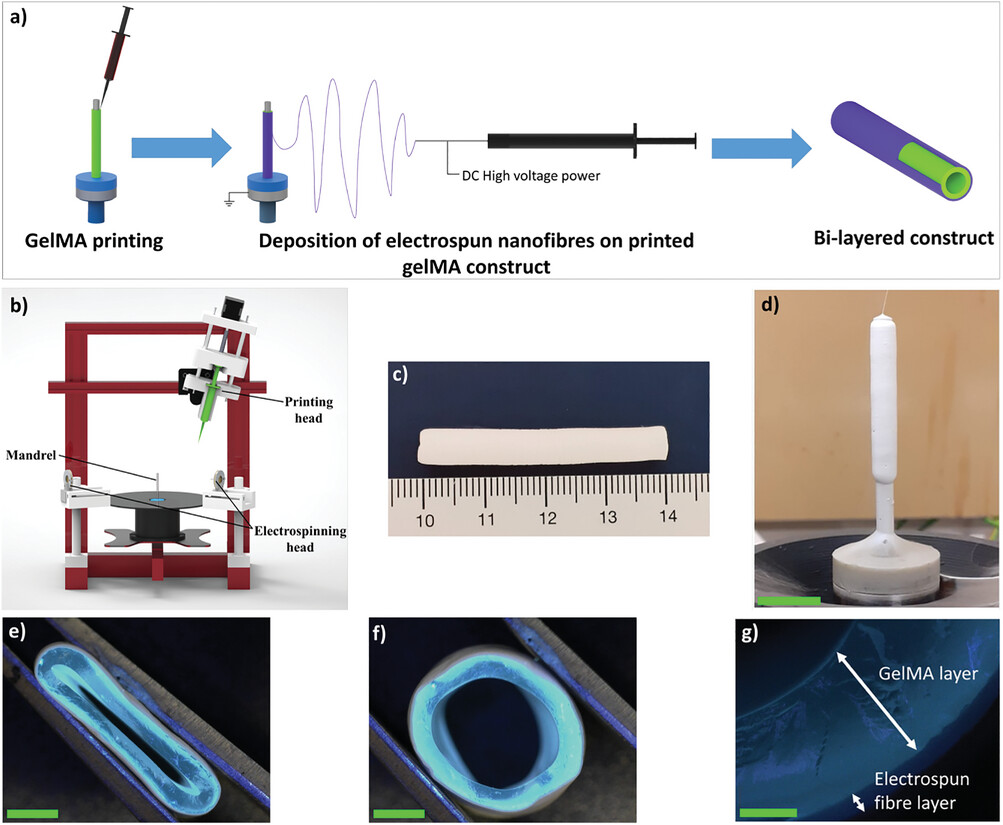
�w�S������ gelMA ��ֲ�����������a) �w�S������ gelMA �Y(ji��)��(g��u)���첽�Eʾ��D��b) ���ӡˢ��늼��b�á�c) ȫ�LѪ����ֲ�d)
늼��{���w�S����������� gelMA ��ֲ������ߣ�15 ���ף���e) ʹ�������ȫ���s����ֲ������ߣ�2 ���ף����l(f��)�ɹ�D��f)
�Ƴ�����ϵ�������ȫ�֏͵���ֲ��Y(ji��)��(g��u)�������ߣ�2 ���ף���g) �����Ѫ����ֲ��M����Ĕ�(sh��)�ֈD���@ʾ��(n��i)�� gelMA
�Ӻ��ⲿ늼��w�S�ӣ������ߣ�0.4 ���ף���

���D2
Ѫ����ֲ��ı��Ɖ���������Ԝy����a) ���� Instron 3367 �f��ԇ�C����Ƭ��b) ���Ɖ����yԇ�Ĝyԇ�_��c)
���Ɖ����yԇ���g���w�S���� gelMA ��ֲ��d) ���Ɖ����yԇ����ֲʧ����e) ��ֲ����Ԝy���b�õ�ʾ��D��f) ����Ԝy���b�õ���Ƭ��g)
����Ԝyԇ���g���� 150 mmHg �������� 75/25 PCL/PLCL 늼��{���w�S������ 10% gelMA �Y(ji��)��(g��u)��

���D3
gelMAˮ���z����׃���Ժ��w�S���� gelMA ��ֲ�������yԇ��a)26��C �� gelMA ˮ���z��ճ���S�������ʵ�׃����b)22��24 ��
26��C �� 7.5% gelMA ��ճ���S�������ʵ�׃����c) 26��C �� gelMA ˮ���z�ă��͓ܺp��ģ���S���l�ʵ�׃�����w�S����
d) 7.5%��e) 10% �� f) 12% gelMA ��ֲ��ĈA�ܑ���-��׃�������w�S���� g) 7.5%��h)10% �� i) 12%
gelMA ��ֲ��Ŀv����-��׃������j) �w�S���� gelMA ��ֲ��ĈA�ܷ������ģ���� k) �w�S���� gelMA
��ֲ���ڿv��ė���ģ����l) �w�S���� gelMA ��ֲ�����ȡ�m) �w�S���� gelMA ��ֲ��v�ȣ�***��p <
0.0001��**��p < 0.001��*��p < 0.05��NS�����@������
���D4 �w�S���� gelMA
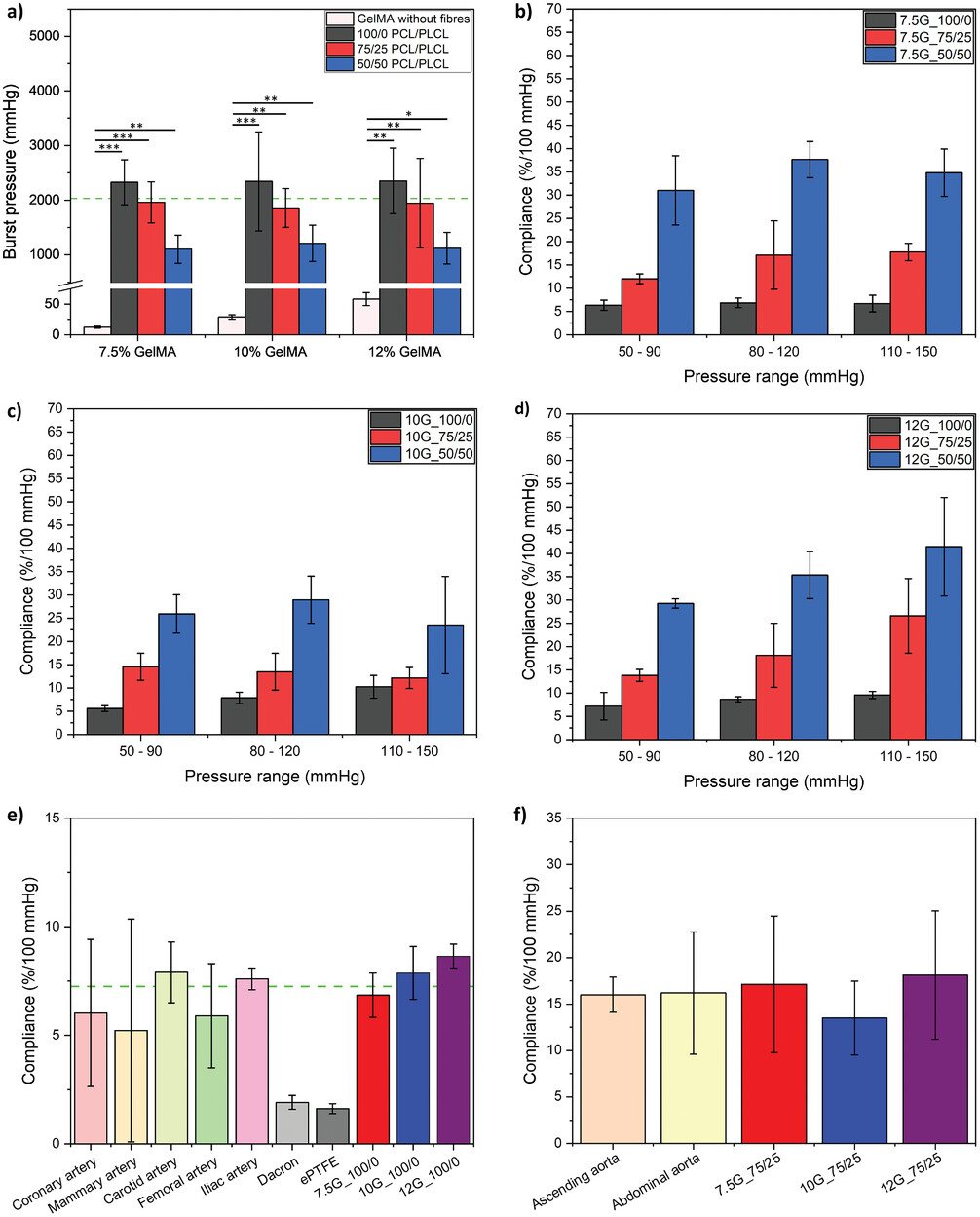
��ֲ��ı��Ɖ�����협��Ԕ�(sh��)��(j��)��a) PCL/PLCL �w�S���� gelMA
��ֲ��ı��Ɖ������Gɫ̓���@ʾСֱ�����}��ƽ�����Ɖ���(***��p < 0.001��**��p < 0.01��*��p <
0.05)��b) 7.5%��c) 10% �� d) 12% PCL/PLCL �w�S���� gelMA ��ֲ���협��ԡ�e) ��80�C120
mmHg ����������(n��i)����Ȼ���Ԅ��}�c���� 100/0 PCL/PLCL �w�S������ gelMA
��ֲ���협��Ա��^���Gɫ̓���@ʾСֱ��Ѫ����ֲ���Ŀ��협���ֵ�� f) �� 80�C120 mmHg ����������(n��i)����Ȼ���Ԅ��}�c���� 75/25
PCL/PLCL �w�S������ gelMA ��ֲ���협��Ա��^��
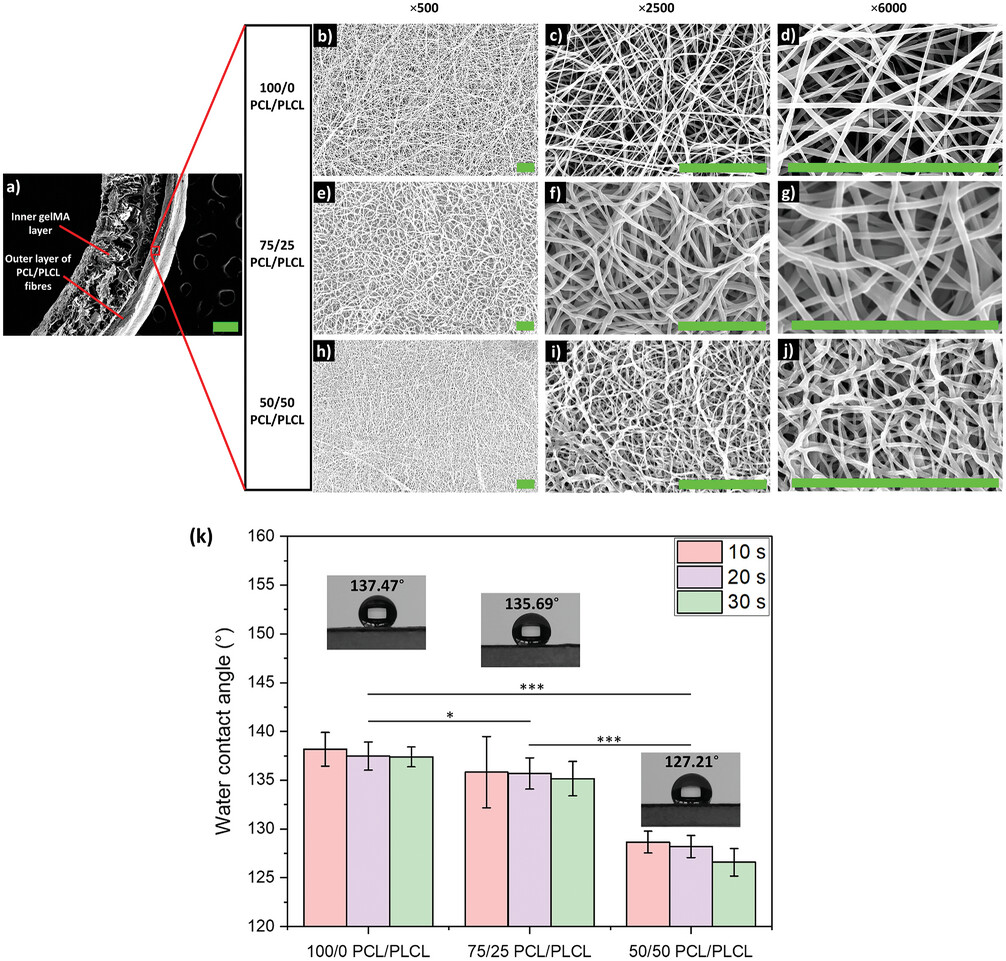
���D5 �w�S���� gelMA ��֦����^�Y(ji��)��(g��u)��늼��{���w�S�ĝ����ԡ�a) �p���w�S����
gelMA �Y(ji��)��(g��u)�� SEM �D�����ߣ�250 µm����100/0 PCL/PLCL 늼��{���w�S�� SEM �D�Ŵ�(sh��)�� b)
��500��c) ��2500��d) ��6000��75/25PCL/PLCL 늼��{���w�S�� SEM �D�Ŵ�(sh��)��e) ��500��f)
��2500��g) ��6000��50/50 PCL/PLCL 늼��{���w�S�� SEM �D�Ŵ�(sh��)�� h) ��500��i)
��2500��j)��6000�������ߣ�20 µm���� k��ˮ���|�Ǘl�ΈD��***��p < 0.001��*��p <
0.05�������а���ÿ�N��r�µĵ���ˮ�ΈD��
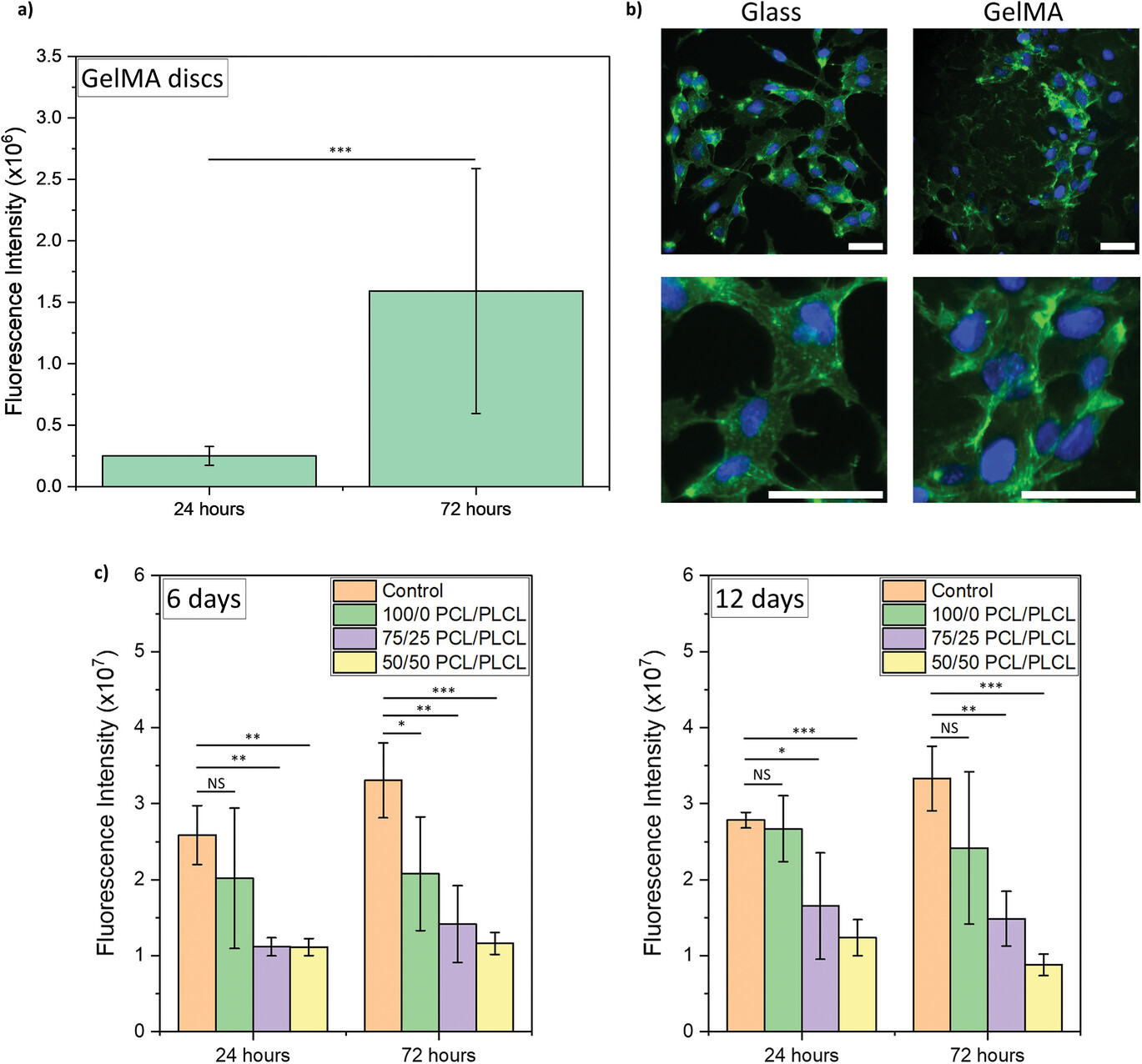
���D6 gelMA �� PCL/PLCL 늼��w�S�ļ��������Է�����a) �u�� 72
С�r��(n��i) gelMA �A�P�ϵ� HUVEC ������*** p �� 0.001��b) �ڲ����� gelMA �����B(y��ng)�� HUVEC
�Ĵ��������ߟɹ�D��Ⱦɫ�� VE-cadherin���Gɫ���� DAPI���{ɫ�����������ߣ�50 µm����c) ��¶��늼��w�S�������B(y��ng)����
HUVEC ������֧�������B(y��ng)���з��� 6 ��� 12 �졣* p �� 0.05��** p �� 0.01��*** p �� 0.001��NS
���@����
3D ��ֲ��ĺ�ȷ�����ֱ�� 1 �� 40 ���ף��ɝM����N���������������`������ζ�����������p���������w���о�����һ�A�Ό��漰�о��@ЩѪ���ڄ������ϵ�ʹ����r���c�۶�����W���_˹���о����������S���M�����wԇ�۶�����W���̌WԺ����Ҫ���� Faraz Fazal ��ʿ�f�����҂��Ļ�ϼ��g(sh��)��M�������йܠ�Y(ji��)��(g��u)�������_�����µĺ������d�^�Ŀ����ԡ����۶�����W���̌WԺ��ϯ�о��T Norbert Radacsi ��ʿ�f�����҂����о��ɹ���Q��Ѫ�ܽM�������I(l��ng)���L�ڴ��ڵ�����(zh��n)�������a(ch��n)��һ�N�����c����o�}���Ƶ��������W���ԵČ��ܡ����˳��m(x��)��֧�ֺͺ�����������Ѫ�ܼ��������ί�������Ը�����ܕ��ɞ�F(xi��n)������
(؟�ξ���admin)
��һƪ���۶�����W�о��ˆT����3D��ӡѪ�ܸ������K������g(sh��)Ч��
��һƪ���H1С�r��KSCAN-Magic �����{�S4������ˮ݆�C�~Ƭ���S�z�y
��һƪ���H1С�r��KSCAN-Magic �����{�S4������ˮ݆�C�~Ƭ���S�z�y
���P(gu��n)��(n��i)��
 649��Ԫ��Revopointȫ��Me
649��Ԫ��Revopointȫ��Me 649��Ԫ��Revopointȫ��Re
649��Ԫ��Revopointȫ��Re �K����(li��n)�������WԺ�Ƴ���
�K����(li��n)�������WԺ�Ƴ��� �F���������F���t(y��)��Ժ�ǿ�
�F���������F���t(y��)��Ժ�ǿ� �㽭ʡ�����t(y��)Ժ/�㽭��W
�㽭ʡ�����t(y��)Ժ/�㽭��W ADNOC Gasʹ��3D��ӡ����
ADNOC Gasʹ��3D��ӡ����
- ��649��Ԫ��Revopointȫ��MetroX 3D����
- ��649��Ԫ��Revopointȫ��Revopoint Metr
- ���K����(li��n)�������WԺ�Ƴ�����3D��ӡģ��
- ���F���������F���t(y��)��Ժ�ǿ��[���F꠳ɹ�
- ���㽭ʡ�����t(y��)Ժ/�㽭��W�Fꠣ����ܸ�
- ��ADNOC Gasʹ��3D��ӡ���������P(gu��n)�I��Q
- ��SpaceX��������Ş����ل�(chu��ng)�o䛣�����3D
- �����a(ch��n)�մ�3D��ӡ�˹����ޏͣ������Ƽ���
����(n��i)��
- ��649��Ԫ��Revopointȫ��MetroX 3D����
- ��649��Ԫ��Revopointȫ��Revopoint Metr
- ���K����(li��n)�������WԺ�Ƴ�����3D��ӡģ��
- ���F���������F���t(y��)��Ժ�ǿ��[���F꠳ɹ�
- ���㽭ʡ�����t(y��)Ժ/�㽭��W�Fꠣ����ܸ�
- ��ADNOC Gasʹ��3D��ӡ���������P(gu��n)�I��Q
- ��SpaceX��������Ş����ل�(chu��ng)�o䛣�����3D
- �����a(ch��n)�մ�3D��ӡ�˹����ޏͣ������Ƽ���
- ��3D��ӡ�����NƬ������С���ӡ�����
- ������é˹ˇ�g(sh��)��W�W����(chu��ng)������������
���]��(n��i)��
���c��(n��i)��
- ��3D��ӡ��������3D��ӡ�P���������ij���
- ����3D��ӡ�C�����b���ˣ�����3d��ӡ��һ
- ���Լ�������һ�_ֻ��20��Ԫ��3D��ӡ��
- ���֙C��ע���ˣ��Ø�ݮ��+3D��ӡ�C����
- ���P�c3D��ӡ���ޏ�������E�еĽ�(j��ng)�䰸��
- ���D�⣺3D��ӡ�������a(ch��n)����
- ��SOLS��˾�l(f��)���ɶ��Ƶ�3D��ӡ�C��Ь�|
- ��ӯ��(chu��ng)3D��ӡ������(j��ng)�䰸������
- ��10�����ص�3D��ӡ���裬����һ������ϲ
- ��3D��ӡ���҃�(n��i)�b�đ��ã��cȼ�㌦���g


 �炐�ȁ���W����
�炐�ȁ���W���� ʧȥ1/3����,���
ʧȥ1/3����,��� 3D��ӡܛƤ�|����
3D��ӡܛƤ�|���� 3D��ӡ��Q������
3D��ӡ��Q������ ���ܲ����¡����T
���ܲ����¡����T �����\��Ʒ��Jack
�����\��Ʒ��Jack

