����ʳƷˎ������֔M�l(f��)��3D��ӡ�t(y��)���O��Č���Ҏ(gu��)�t
��Ŀǰڅ�݁�����3D��ӡ���g�����҂��M��һ�����Ի��ĕr�������S�t(y��)��������t(y��)����ˎ�������ơ������t(y��)���O���ˎ������Ǟ鲡�˄�(chu��ng)���Ҏ(gu��)ģ���a(ch��n)�Įa(ch��n)Ʒ��

��������3D��ӡ���t(y��)���O����횫@��ʳƷ��ˎ������֣�FDA�����ʺ��N�ۡ�Ŀǰ����3D��ӡ�O����u�r�^�̷dz������ĕr������@��¼��g�]�о��w�ęz��˜ʡ�����ʳƷ��ˎ����������ڞ�3D��ӡ�O������Ҏ(gu��)������5�¹��_�l(f��)����һƪ�����������O��ļ��g����IJݸ塣

�@Щ�ʄt���䌍���H�ܞ�3D��ӡ�t(y��)���O����(chu��ng)���İl(f��)չ���g��߀����a(ch��n)Ʒ���_�l(f��)���������ṩ�@����ָ��������ʳƷ��ˎ��������ѽ�(j��ng)�u����������85��3D��ӡ�t(y��)���O���1��3D��ӡ̎��ˎ������߀��̎�����ࡣ

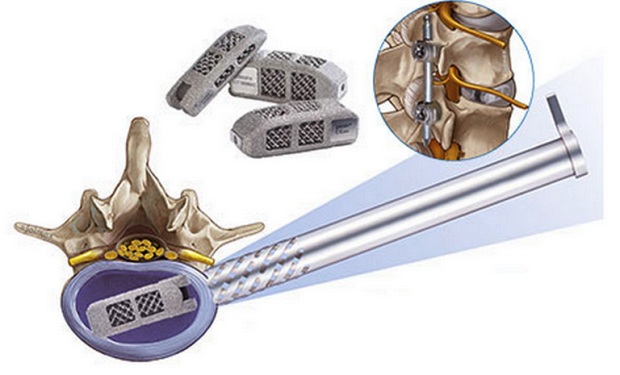
3D��ӡ�������ֲ�����DZ�����ʳƷ��ˎ����������ʵ��O��֮һ�����������m�����˵����w�Լ��ض���������g��е�����Ԏ����t(y��)���ӿ�ֲ�������g�^�̵ġ�

���е�(li��n)��C����ָ�����ͨ�����Բݸ����ʽ���Ρ��������l(f��)����Ȼ�����ИI(y��)�ķ�����ݔ����Կ�����3D��ӡ���g�Ա��J���Ǿo�����Ҳ���l(f��)չ�ġ����Ќ�ԓ���g����Ҋ�ͷ���������ʳƷ��ˎ������ֶ�ҕ��dz���Ҫ�ą����Y�ϣ����������_������ݰ������ڴ��@�ø���ķ�����Ȼ������Ŀǰ��ֻ�յ���3�l�uՓ��
����Ҏ(gu��)�t������cָ����3D��ӡ�ИI(y��)��ÿһ�l�������o����Ҫ�����̹�ʵ��f�����@ЩҎ(gu��)�t����֮ǰ��Ҫ�����ѽ�(j��ng)����֮�������׃��ؓ؟3D��ӡ�t(y��)����е��ֲ��������g���ߵĹ�˾��ԓ�Ѓ�(y��u)�Ȳ鿴�ݰ��ę��������������I(y��)�I�����I(y��)��ʿ��������á�
(؟�ξ���admin)
 �O�⠖�֣����߭h(hu��n)������3D
�O�⠖�֣����߭h(hu��n)������3D ����܊���������켼�g�l(f��)չ
����܊���������켼�g�l(f��)չ ��SLA��3D��ӡ�C�F�w�˜�
��SLA��3D��ӡ�C�F�w�˜� 3D��ӡ�t(y��)����е���P�˜���
3D��ӡ�t(y��)����е���P�˜��� ���Ų�������3D��ӡ��ĩ��
���Ų�������3D��ӡ��ĩ�� ȫ���ׂ���������3D��ӡϵ
ȫ���ׂ���������3D��ӡϵ
- ���O�⠖�֣����߭h(hu��n)������3D��ӡ������ӭ
- ������܊���������켼�g�l(f��)չҎ(gu��)��
- ����SLA��3D��ӡ�C�F�w�˜ʡ����Ϻ�¡��
- ���V�|ʡ�P��������c�������족�ش�
- ��3D��ӡ�t(y��)����е���P�˜��ƶ����ЙzԺ��
- �����Ų�������3D��ӡ��ĩ�������|(zh��)������
- ��ȫ���ׂ���������3D��ӡϵ�y(t��ng)���칤ˇ��
- ����������AM��ANSI�l(f��)�����°汾��������
- ���O�⠖�֣����߭h(hu��n)������3D��ӡ������ӭ
- ������܊���������켼�g�l(f��)չҎ(gu��)��
- ����SLA��3D��ӡ�C�F�w�˜ʡ����Ϻ�¡��
- ���V�|ʡ�P��������c�������족�ش�
- ��3D��ӡ�t(y��)����е���P�˜��ƶ����ЙzԺ��
- �����Ų�������3D��ӡ��ĩ�������|(zh��)������
- ��ȫ���ׂ���������3D��ӡϵ�y(t��ng)���칤ˇ��
- ����������AM��ANSI�l(f��)�����°汾��������
- �����Ų���ؔ�����l(f��)��2018�깤�I(y��)�D(zhu��n)������
- �����ʡ3D��ӡ�a(ch��n)�I(y��)���g��(chu��ng)��(li��n)�����_2017
- ���������c�аl(f��)Ӌ��2017�����������c���
- ���������3D��ӡ�a(ch��n)�I(y��)�l(f��)չ·��
- �����Ų���֧��3D��ӡ�����a(ch��n)�I(y��)���g��(chu��ng)����
- ���Ƽ��������������c���2017����Ŀ��
- ���Ƽ����l(f��)�������������c���2016�����
- ������Ժӡ�l(f��)��ʮ���塱Ҏ(gu��)�� ����3D��ӡ
- ������ȫ��3D��ӡ��������һ�[
- ���e�����ˣ�3D��ӡ���gASTM F2792�˜ʁ�
- ����ˏ���Ҫ�vԒ���á���(li��n)�W(w��ng)+������3D
- �����Ų��C������ʮ���塱�l(f��)չҎ(gu��)���� 3D


 ���ʡ3D��ӡ�a(ch��n)�I(y��)
���ʡ3D��ӡ�a(ch��n)�I(y��) �������c�аl(f��)Ӌ��
�������c�аl(f��)Ӌ�� ��ȫ������ԺУ��
��ȫ������ԺУ�� ����ʳƷˎƷ�O(ji��n)��
����ʳƷˎƷ�O(ji��n)��

