��ACS AMI����3D��ӡ֧�ܳ��m(x��)ጷŵ������ɴ��M(j��n)��������
�r(sh��)�g��2023-12-12 09:53 ��Դ��EngineeringForLife ���ߣ�admin ��x����
ͨ�^�{(di��o)��(ji��)����(x��)��������(qi��ng)�ɹ���һ�N��Q��(d��ng)ǰ�ޏ�(f��)��ȱ�p��������(zh��n)���·�����Ȼ�����P(gu��n)�ڹ��γ��^��������(x��)�����Vϵ��(x��)��֮�g����������кܶ�δ֪�����⣬�����������֧�ܵķ���Ҳȱ����Ч���{(di��o)��(ji��)�@�N��?d��ng)_�Դ��M(j��n)�����ϡ�

���ڴˣ�Ӣ���Z���h��W(xu��)Amir EngineeringForLife��Jing Yang�״��о��˾��ɼ�(x��)�����g���|(zh��)�ɼ�(x��)����MSCs���ڹ����B(y��ng)�r(sh��)��ͨ�^�����S��3D����ӡ֧���г��m(x��)ጷ�һ�N���ʹٳɹ�ˎ��������ɣ�֮�g������ã��C��ʹ��ˎ��ጷ�֧�܁��{(di��o)��(ji��)�װY������(qi��ng)�������ĝ�����
����Ҫ�c(di��n)��
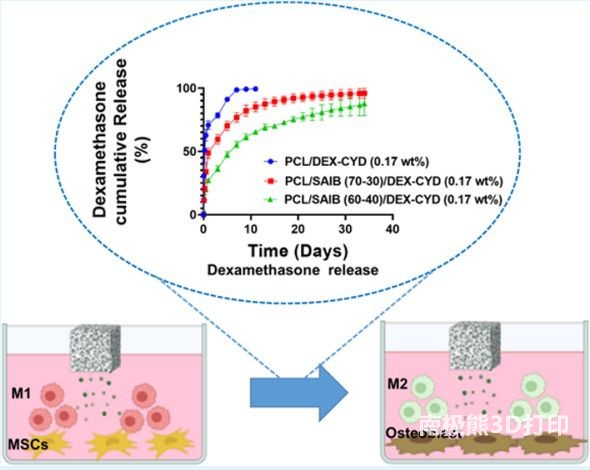
��1�����о��ɹ����a(ch��n)3D��ӡ֧�ܣ��Ը����m(x��)�ķ�ʽ�ڼ{������(n��i)ጷŵ������ɡ�
��2����MSC-���ɼ�(x��)�������B(y��ng)�^���У��p���Ե������ɼȴ��M(j��n)�ɹǷֻ��������ƴ���M1���ɼ�(x��)����
��3��M1���ɼ�(x��)�������څ��c�ɹǣ����@�N�����S��p������M1���ɼ�(x��)���ijɹ����Ï�(qi��ng)��M0�ɹǼ�(x��)����
��4���������ɴ��M(j��n)BMP-2�������࣬��M1���ɼ�(x��)�����M(j��n)BMP-2���ڶ���M0���ɼ�(x��)����
�C�ϣ����о���(qi��ng)�{(di��o)�˿�ֲ��֧�ܿ���ጷ�ˎ���ڹ��������^�����{(di��o)��(ji��)�ɹǷֻ��;��ɼ�(x��)�������B(t��i)�ĝ�����
����Դ��
https://pubs.acs.org/10.1021/acsami.3c09774

���ڴˣ�Ӣ���Z���h��W(xu��)Amir EngineeringForLife��Jing Yang�״��о��˾��ɼ�(x��)�����g���|(zh��)�ɼ�(x��)����MSCs���ڹ����B(y��ng)�r(sh��)��ͨ�^�����S��3D����ӡ֧���г��m(x��)ጷ�һ�N���ʹٳɹ�ˎ��������ɣ�֮�g������ã��C��ʹ��ˎ��ጷ�֧�܁��{(di��o)��(ji��)�װY������(qi��ng)�������ĝ�����

����Ҫ�c(di��n)��
��1�����о��ɹ����a(ch��n)3D��ӡ֧�ܣ��Ը����m(x��)�ķ�ʽ�ڼ{������(n��i)ጷŵ������ɡ�
��2����MSC-���ɼ�(x��)�������B(y��ng)�^���У��p���Ե������ɼȴ��M(j��n)�ɹǷֻ��������ƴ���M1���ɼ�(x��)����
��3��M1���ɼ�(x��)�������څ��c�ɹǣ����@�N�����S��p������M1���ɼ�(x��)���ijɹ����Ï�(qi��ng)��M0�ɹǼ�(x��)����
��4���������ɴ��M(j��n)BMP-2�������࣬��M1���ɼ�(x��)�����M(j��n)BMP-2���ڶ���M0���ɼ�(x��)����
�C�ϣ����о���(qi��ng)�{(di��o)�˿�ֲ��֧�ܿ���ጷ�ˎ���ڹ��������^�����{(di��o)��(ji��)�ɹǷֻ��;��ɼ�(x��)�������B(t��i)�ĝ�����
����Դ��
https://pubs.acs.org/10.1021/acsami.3c09774
(؟(z��)�ξ���admin)
��һƪ���ݿ��O(sh��)Ӌ(j��)��ʹ�ÿɻ��ղ���3D��ӡ��������ˇ�g(sh��)��Ʒ�c�ɳ��m(x��)���(sh��)�F(xi��n)�ں�
��һƪ������3D��ӡ���K��Ĥ����īˮ��δ�����������������Kȱ�����g(sh��)
��һƪ������3D��ӡ���K��Ĥ����īˮ��δ�����������������Kȱ�����g(sh��)
���P(gu��n)��(n��i)��
 Vertico�Ƴ��ɳ��m(x��)ģ�K��3
Vertico�Ƴ��ɳ��m(x��)ģ�K��3 ����ɣ�Ǵ�W(xu��)�аl(f��)3D��ӡ��
����ɣ�Ǵ�W(xu��)�аl(f��)3D��ӡ�� ���Ȳ�ͬ��Դ�ljK��ֲ�
���Ȳ�ͬ��Դ�ljK��ֲ� ��؛���ڡ��������M(f��i)���p��
��؛���ڡ��������M(f��i)���p�� ���������x���\(y��n)���b�䣺Ca
���������x���\(y��n)���b�䣺Ca ����CoAspire�cDivergent
����CoAspire�cDivergent
- ��Vertico�Ƴ��ɳ��m(x��)ģ�K��3D��ӡ����DIA
- ������ɣ�Ǵ�W(xu��)�аl(f��)3D��ӡ�ɴ����O(sh��)�䣺ͨ
- �����Ȳ�ͬ��Դ�ljK��ֲ�3D��ӡ������
- ����؛���ڡ��������M(f��i)���p�룬��⁺Ͻ�3D
- �����������x���\(y��n)���b�䣺Carbon�cReusch
- ������CoAspire�cDivergent��˾(li��n)���аl(f��)3
- ��ChristianaCare 3D��ӡ���������ί�Ƥ
- ��Alquist 3D����3D��ӡ���g(sh��)��Ч����֠�
����(n��i)��
- ��Vertico�Ƴ��ɳ��m(x��)ģ�K��3D��ӡ����DIA
- ������ɣ�Ǵ�W(xu��)�аl(f��)3D��ӡ�ɴ����O(sh��)�䣺ͨ
- �����Ȳ�ͬ��Դ�ljK��ֲ�3D��ӡ������
- ����؛���ڡ��������M(f��i)���p�룬��⁺Ͻ�3D
- �����������x���\(y��n)���b�䣺Carbon�cReusch
- ������CoAspire�cDivergent��˾(li��n)���аl(f��)3
- ��ChristianaCare 3D��ӡ���������ί�Ƥ
- ��Alquist 3D����3D��ӡ���g(sh��)��Ч����֠�
- ��CoAspire��Divergent���g(sh��)��˾��(sh��)�F(xi��n)3D��
- ��VICIS(li��n)��Carbon�Ƴ�NFL피�3D��ӡ�^��
���]��(n��i)��
���c(di��n)��(n��i)��
- ��3D��ӡ��������3D��ӡ�P���������ij���
- ����3D��ӡ�C(j��)�����b���ˣ�����3d��ӡ��һ
- ���ƌW(xu��)���_�l(f��)��3D��ӡ���ԡ������족늳�
- ��600mm��ߴ�SLS 3D��ӡ�C(j��)��o�˾�܇܇
- ��Curiteva��(b��o)��Q3D��ӡ��С��PEEK�g�P
- ���Լ�������һ�_ֻ��20��Ԫ��3D��ӡ��
- ���ձ�����ȫ������3D��ӡ��܇վ
- ���P�c(di��n)3D��ӡ���ޏ�(f��)������E�еĽ�(j��ng)�䰸��
- ���֙C(j��)��ע���ˣ��Ø�ݮ��+3D��ӡ�C(j��)����
- ���D�⣺3D��ӡ�������a(ch��n)����


 �ջݹ�˾�Ƴ��µ�
�ջݹ�˾�Ƴ��µ� �ÿ��_˹������
�ÿ��_˹������ ��܊���M(j��n)�h(yu��n)��3D��
��܊���M(j��n)�h(yu��n)��3D�� 3D��ӡ�ğύ�Q��
3D��ӡ�ğύ�Q�� 3D��ӡ��(sh��)�F(xi��n)��̶�
3D��ӡ��(sh��)�F(xi��n)��̶� �炐�ȁ���W(xu��)����
�炐�ȁ���W(xu��)����

